Protocole Immunohistochimie - Méthode Avidine/Biotine Complexe (ABC)
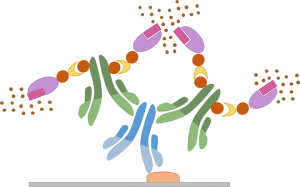
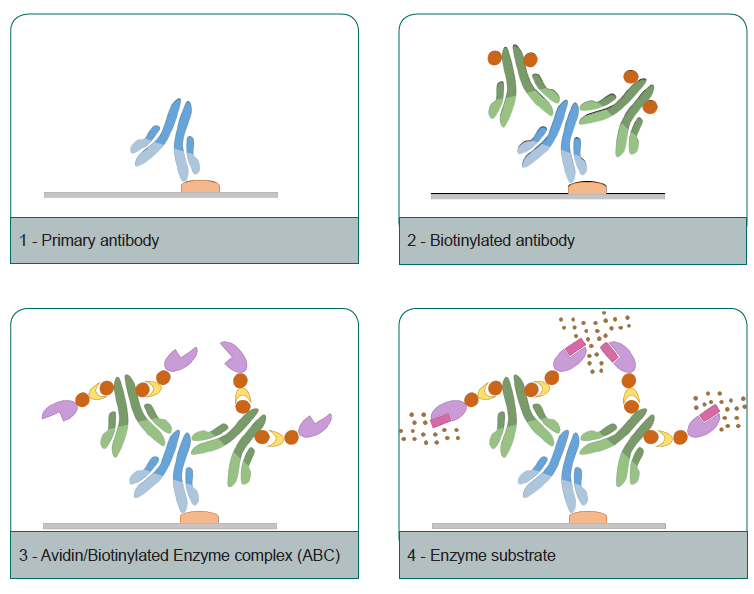
Le principe des kits de detection ABC repose sur l'affinité de l'avidine (ou de la streptavidin) pour la biotin. En effet, l'abbréviation ABC signifie Avidin/Biotin Complex.
En générale, les kits de détection ABC sont composés de :
- D'un anticorps secondaires biotinylé
- D'un complexe Avidine / Enzyme
Les kits peuvent contenir ou non les tampons de blocages et de dilutions et le substrat en fonction des formats.
I. Matériels requis
Réactifs
- Un (ou plusieurs) anticorps primaire couplé(s) ou non et spécifiques de votre(s) molécule(s) d'intérêt
- Kit de révélation
- Chromogène
Tampons
- Xylène
- Bains d'alcool à 70%, 80%et 95%
- Péroxyde d'hydrogène (H2O2)
- Tris EDTA, Tris HCl
- Tween-20
Réactifs
- Un (ou plusieurs) anticorps primaire couplé(s) ou non et spécifiques de votre(s) molécule(s) d'intérêt
- Kit de révélation
- Chromogène
Tampons
- Xylène
- Bains d'alcool à 70%, 80%et 95%
- Péroxyde d'hydrogène (H2O2)
- Tris EDTA, Tris HCl
- Tween-20
II. Durée de l'expérimentation
- 10 min de blocage des péroxydases
- 30 min de démasquage antigénique (si nécessaire)
- 30-60 min d'incubation avec l'anticorps primaire
- 10 min d'incubation avec l'anticorps secondaire biotinylé
- 10 min d'incubation avec le conjugué streptavidine / Peroxidase
- 5 min de chromogène
- 5 min de chromogène
- Coloration Hématoxyline / Eosine (optionnel)
- TOTAL : 2-3 heures
- TOTAL : 2-3 heures
III. Mode opératoire
- Blocage des peroxydases endogènes : Appliquer 2 gouttes (100 µl), ou un volume suffisant pour couvrir la coupe de tissu, de réactif de blocage des peroxydases endogènes (solution à 3%de H2O2) et incuber quelques minutes. Rincer la lame à l'eau distillée.
- Démasquage de l'antigène (traitement HIER) en fonction de l'anticorps primaire utilisé : Procéder au démasquage comme indiqué sur la fiche technique de l'anticorps primaire puis rincer 3 x 2 min avec du PBS.
- Pré-blocage : Appliquer 2 gouttes (100 µl), ou un volume suffisant pour couvrir la coupe de tissu, de solution de pré-blocage et incuber 10 min. Retirer la solution mais ne pas rincer.
- Anticorps primaire : Les utilisateurs doivent optimiser la dilution et le temps d'incubation en fonction de l'anticorps utilisé. Appliquer 2 gouttes (100 µl), ou un volume suffisant pour couvrir la coupe de tissu, d'anticorps primaire et incuber 30-60 min. Rincer avec du PBS 3 x 2 min.
- Anticorps secondaire : Appliquer 2 gouttes (100 µl), ou un volume suffisant pour couvrir la coupe de tissu, d'anticorps secondaire biotinylé et incuber pendant 10 min. Rincer 3 x 2 min avec du PBS
- Conjugué Streptavidine-HRP : Appliquer 2 gouttes (100 µl), ou un volume suffisant pour couvrir la coupe de tissu, de conjugué Streptavidine-HRP et incuber pendant 10 min. Rincer 3 x 2 min avec du PBS
- Substrat / Chromogène : Ajouter 1 goutte ou 2 gouttes (pour une meilleure sensibilité et contraste) de chromogène concentré à 1 ml de substrat. Bien agité, protéger de la lumière et utiliser dans les 5 heures. Appliquer 2 gouttes (100 µl), ou un volume suffisant pour couvrir la coupe de tissu, de solution chromogène et incuber 5 minutes. Rincer 3 x 2 min avec de l'eau distillée.
- Hématoxyline : Contre-colorer l'échantillon avec 2 gouttes (100 µl), ou un volume suffisant pour couvrir la coupe de tissu, et incuber pendant 10-20 sec. Rincer abondamment pendant 1-2 min avec de l'eau distillée. Mettre les lames dans du PBS jusqu'à l'obtention d'une coloration bleue (30-60 sec).
- Montage : Suivre la fiche technique du liquide de montage.
Notes :
- La fixation, l'épaisseur des coupes de tissu, le démasquage de l'antigène ainsi que les dilutions et temps d'incubation de l'anticorps primaire peuvent affecter les résultats de façon significative. Les utilisateurs doivent prendre en considération tous les facteurs et déterminer les conditions optimales.
- La coloration du tissu est dépendante des traitements effectués sur les tissus avant l'immunohistochimie. Une mauvaise préparation des tissus peut entraîner des faux négatifs et des résultats très divergents d'une expérience à l'autre.
- Si vous utilisez des kits contenant tous les réactifs pour l'IHC, ceux ci sont testés ensemble pour assurer les meilleurs résultats possibles. Il est donc conseiller de ne pas mélanger les réactifs de différents lots.
- Ne pas laisser les échantillons de tissu sécher pendant toute la durée du protocole et utiliser une chambre humide pour les incubations.

